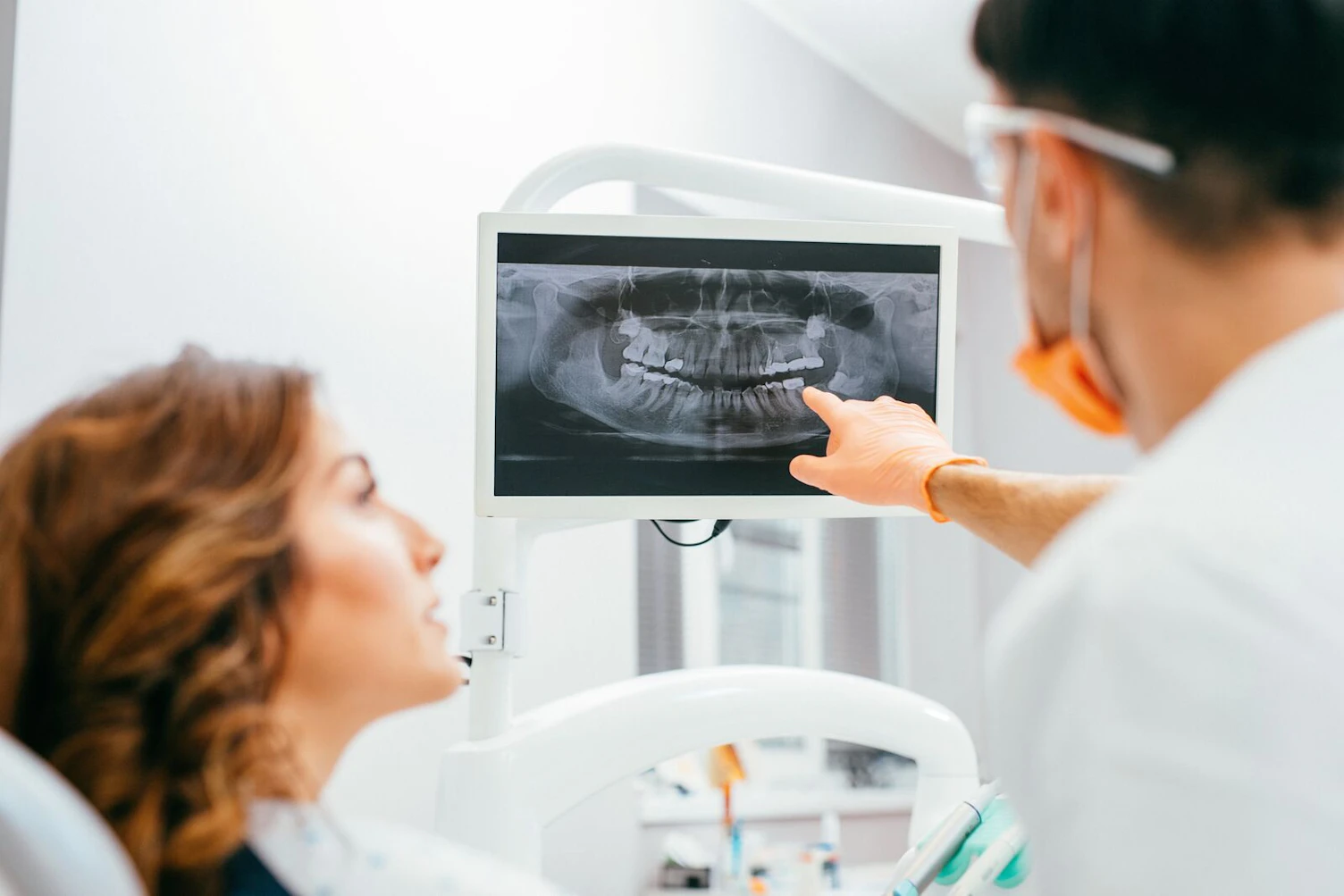
I dispositivi odontoiatrici coprono un ampio spettro, che va dagli impianti agli strumenti, dai filler ai materiali da impronta. Per garantire che l'organismo notificato UE o l'organismo approvato del Regno Unito sia qualificato per esaminare un dispositivo specifico, i dispositivi vengono classificati e raggruppati in base all'uso previsto o alle tecnologie impiegate nel dispositivo. Per comodità del produttore, utilizziamo un unico sistema di codifica sia per l'UE che per il Regno Unito. Ai dispositivi vengono assegnati i codici in base all'elenco dei codici MDR accessibile al pubblico dal regolamento di attuazione (UE) 2017/2185 della Commissione del 23 novembre 2017. Ciò è ulteriormente spiegato dal documento MDCG 2019-14 del Gruppo di coordinamento dei dispositivi medici per identificare e classificare i dispositivi dentali. Questi possono includere:
- MDN 1103: impianti dentali non attivi e materiali dentali, che comprendono dispositivi quali impianti dentali, otturazioni dentali e otturazioni permanenti di guttaperca per canali radicolari, monconi, corone dentali, faccette e resine composite, tra gli altri
- MDN 1202: Dispositivi non impiantabili progettati per la somministrazione, la canalizzazione e la rimozione di sostanze. Copre elementi come i componenti non attivi dei dispositivi di aspirazione o degli aspirasaliva, tra gli altri
- MDN 1208: Questa categoria comprende strumenti non attivi e non impiantabili come scaler dentali, specchi, escavatori, brunitori e curette
- MDN 1209: Materiali dentali inattivi e non impiantabili, come soluzioni mordenzanti, apparecchi ortodontici, cementi a breve termine e materiali da impronta, tra gli altri
Per supportare valutazioni efficaci della conformità, i dispositivi sono anche raggruppati utilizzando la Nomenclatura europea dei dispositivi medici (EMDN) per l'UE, o la Nomenclatura globale dei dispositivi medici (GMDN) nel Regno Unito, per identificare e classificare i dispositivi dentali che possono essere valutati insieme.